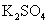2025年云南中考化学试题及答案
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Ga-70
一、选择题:本题共20小题,每小题2分,共40分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 下列云南传统节日活动主要涉及化学变化的是
A. “火把节”点火把B. “泼水节”洒吉水
C. “三月街”观赛马D. “扎勒特”跳铓鼓
2. 空气中能供给呼吸的气体是
A. 氮气B. 氧气C. 稀有气体D. 二氧化碳
3. 农产品种植需要化肥,下列属于氮肥的是
A. ![]() B.
B. ![]() C.
C. ![]() D. KCl
D. KCl
4. 下列是配制稀硫酸并探究其化学性质的部分实验操作,其中正确的是
A. 稀释浓硫酸 B. 测pH
B. 测pH
C. 取锌粒 D. 倾倒液体
D. 倾倒液体
5. 下列宏观事实的微观解释不正确的是
A. 端午粽飘香——分子不断运动
B. 水沸腾把壶盖顶开——分子体积变大
C. 1g水中约含有![]() 个水分子——分子质量很小
个水分子——分子质量很小
D. 石蜡熔化——分子种类不变
6. 氟元素(F)是维持正常生命活动必需的微量元素。下列表示2个氟原子的是
A. 2FB. 2F-C. F2D. 2F2
7. “健康饮食·健康中国·健康人生”。下列不符合这一理念的是
A. 适量补碘预防甲状腺肿大B. 适量运动,增强体质
C. 用甲醛溶液浸泡海鲜保鲜D. 合理膳食,均衡营养
8. 云南是植物王国,下列植物适宜在碱性土壤中生长的是
选项 | A | B | C | D |
植物 | 薄荷 | 草莓 | 水仙花 | 玫瑰 |
适宜pH | 7~8 | 5~6.9 | 6~6.5 | 6~7 |
A. AB. BC. CD. D
9. 下列物质不属于溶液的是
A. 碘酒B. 糖水C. 盐水D. 泥水
10. 2025年我国环境日的主题是“美丽中国我先行”。下列与该主题不相符的是
A. 开发利用清洁能源B. 倡导绿色出行
C. 减少使用一次性餐具D. 露天焚烧垃圾
11. 全新芯片材料硒氧化铋(Bi2O2Se)中的铋元素在周期表中的信息如图所示。下列有关铋元素说法不正确的是

A. 原子序数为83B. 元素符号为Bi
C. 一个铋原子的质量为209.0gD. 铋是一种金属元素
12. 下列有关碳和碳的氧化物说法不正确的是
A. CO和CO2均可通过C和O2反应得到
B. CO可作燃料,CO2可作气体肥料
C. CO有毒,煤炉上放一壶水能防止煤气中毒
D. 金刚石薄膜可用于集成电路基板散热
13. 下列实验不能达到实验目的的是
| |
A. 探究空气中氧气的含量 | B.探究铁生锈与氧气和水有关 |
| |
C. 验证质量守恒定律 | D. 验证大理石与稀盐酸反应能生成二氧化碳 |
A. AB. BC. CD. D
14. 荷叶作为我国传统中药材之一,具有降脂、止血、清热解毒的功效,其中含有荷叶碱(![]() )。下列说法正确的是
)。下列说法正确的是
A. 荷叶碱中含有氧分子B. 一个荷叶碱分子含有43个原子
C. 荷叶碱由五种元素组成D. 荷叶碱中碳、氢元素质量比为19:21
15. 下列属于复分解反应的是
A. 制备氧化锂生产玻璃电极:
B. 工业制备金属锂:
C. 纽扣电池的工作原理:![]()
D. 制备![]() 生产光学级单晶:
生产光学级单晶:![]()
16. 利用分解和合成探究水的组成的过程,对形成研究物质组成的思路与方法具有重要意义。下列说法不正确的是

A. 图1中,管a、管b产生气体![]() 体积比约为2:1
体积比约为2:1
B. 图2中,观察到干燥烧杯内出现水雾,可知水中一定含有氢元素
C. 两个化学变化过程中,分子、原子种类均发生改变
D. 本探究得出的结论是水由氢、氧元素组成
17. KOH的性质与Ca(OH)2相似。下列对KOH性质的预测不正确的是
A. 能使无色酚酞溶液变红B. 能与![]() 反应
反应
C. 能与![]() 溶液反应D. 能与
溶液反应D. 能与![]() 溶液反应
溶液反应
18. 电石灯是古老的照明工具,原理是利用电石(![]() )与水反应生成可燃性气体,点燃气体用于照明。下列说法正确的是
)与水反应生成可燃性气体,点燃气体用于照明。下列说法正确的是

A. 电石灯利用电石作可燃物B. 点燃是为了提高可燃物的着火点
C. 可通过移动螺母最终使火焰熄灭D. 导管1可长期使用,无需清洁保养
19. 下列实验方案合理的是
选项 | 实验目的 | 实验方案 |
A | 鉴别生理盐水、葡萄糖溶液 | 观察溶液颜色 |
B | 鉴别C、Fe、CuO粉末 | 取样,分别加入足量稀硫酸,观察现象 |
C | 除去 | 加入足量Fe粉,充分反应后过滤 |
D | 除去NaOH溶液中的少量 | 加入适量 |
A. AB. BC. CD. D
20. 捕集![]() 合成尿素
合成尿素![]() ,可实现
,可实现![]() 资源化利用,转化流程如图所示。下列说法不正确的是
资源化利用,转化流程如图所示。下列说法不正确的是

A. 理论上,反应②中合成![]() 需要
需要![]()
B. 理论上,反应③中参加反应的![]() 和
和![]() 的质量比为17:22
的质量比为17:22
C. 该转化流程中,![]() 可循环利用,无需额外补充
可循环利用,无需额外补充
D. 该转化流程中,分子总数减少
二、填空与简答:本题共6小题,化学方程式每空2分,其余每空1分,共30分。
21. 衣食住行是民生之基。
(1)苗族服饰材质以麻为主,麻属于___________有机高分子材料(填“天然”或“合成”)。
(2)哈尼族“七色糯米饭”中的糯米提供的主要营养物质是___________。
(3)生活离不开能源。便携式充电宝给用电器充电时,将化学能转化为___________(填选项)。
A. 热能B. 动能C. 电能D. 光能
(4)芯片是智能汽车的重要部件,其生产过程中可用NF3气体进行蚀刻,该反应的微观示意图如下,则化学方程式为___________。

保护并利用水资源,推进人与自然和谐共生。完成下面小题。
22. 近年来,滇池水环境质量持续改善,逐步实现“人水和谐”的景象。
(1)治理滇池时,用藻车打捞蓝藻,实现藻水分离,该原理与实验操作中的___________类似。
(2)滇池水是当地的自来水水源之一,自来水厂净水过程中,能使水中悬浮杂质较快沉降的是___________(填“活性炭”或“明矾”)。
(3)下列为国家节水标志的是___________(填选项)。
A.  B.
B.  C.
C.  D.
D. 
(4)践行垃圾分类,有助于保护滇池水环境。下列属于有害垃圾的是___________(填选项)。
A. 易拉罐B. 废旧电池C. 塑料瓶D. 废旧纸张
23. 综合利用海洋资源,有助于实现建设海洋强国的战略目标。
(1)浅池蒸发法以太阳能为热源,蒸发海水,获得粗盐。粗盐中的氯化钠由___________(填“分子”“原子”或“离子”)构成。
(2)20℃时,配制100g溶质质量分数为16%的氯化钠溶液用于小麦选种,步骤如图所示。

①实验中,玻璃棒的作用是___________。
②已知20℃时,氯化钠在水中的溶解度为36.0g,则该选种液为20℃时氯化钠的___________(填“饱和”或“不饱和”)溶液。
(3)选种时,将小麦种放入选种液中,劣质种子上浮,优质种子下沉。选种液的溶质质量分数越大密度越大,配制选种液,用量筒量取水时,若俯视读数,可能导致选出的优质麦种数量___________(填“增加”“减少”或“不变”)。
(4)碳纤维增强塑料(CFRP)可用于制造高效率![]() 深海探测器。为适应海洋的特殊环境,该材料应具有的化学性质为___________(任填一条)。
深海探测器。为适应海洋的特殊环境,该材料应具有的化学性质为___________(任填一条)。
绘画是中华优秀传统文化的重要组成部分,许多绘画作品的背后都蕴含着现代化学的智慧。完成下面小题。
24. 阅读短文,回答问题。
《千里江山图》使用天然矿物颜料层层着色,历经千载依然厚重绮丽。
第一层以墨绘之。古人焚烧植物,收集火烟凝成的黑灰制得最早的炭黑。第二层以赭石上红色,其主要成分为Fe2O3.第三、四层均上绿色,此色从石绿取之,石绿的主要成分为![]() 。第五层上青色,此色取自石青,主要成分为
。第五层上青色,此色取自石青,主要成分为![]() 。
。
矿物颜料为《千里江山图》增添了极大的色彩魅力,让这幅古画在历史长河中熠熠生辉。

(1)以墨绘画长久不变色,原因是常温下碳具有___________性。
(2)赭石的主要成分中,金属元素的化合价为___________。工业上也可用赭石和一氧化碳炼铁,其化学方程式为___________。
(3)石绿在一定条件下会转化为石青,其化学方程式为
![]() ,则X的化学式为___________。
,则X的化学式为___________。
25. 现代绘画的红色颜料已很少使用赭石,而是通过化学方法制备)![]() 。例如可用废铁丝(主要含铁和少量氧化铁,其余杂质不参与反应)制得,其工艺流程如图所示。
。例如可用废铁丝(主要含铁和少量氧化铁,其余杂质不参与反应)制得,其工艺流程如图所示。

(1)“酸浸”过程中,可加快化学反应速率![]() 方法有___________(任填一种)。
方法有___________(任填一种)。
(2)“酸浸”过程中,加入过量稀盐酸的目的是___________。
(3)Fe(OH)3高温焙烧得到两种氧化物,化学方程式为___________。
(4)流程中的两次过滤均不能省略,其中“过滤1”不能省略的原因是___________。
26. 临床治疗“胃酸过多症”的抗酸药有氢氧化铝片、碳酸氢钠片、铝碳酸镁片等。抗酸药的标准之一是药物发生疗效时,胃液pH保持在3~5之间最宜,pH过高会导致胃痛等不适症状。回答下列问题。
(1)铝碳酸镁的化学式为![]() ,其中含有___________种非金属元素。
,其中含有___________种非金属元素。
(2)碳酸氢钠俗称___________,治疗胃酸过多时,发生的主要反应的化学方程式为___________。
(3)上述三种药物中,利用中和反应原理治疗胃酸过多症的是___________。
(4)已知铝碳酸镁片是当今的主流抗酸药,为探究铝碳酸镁片相比碳酸氢钠片的优势,实验室用pH=1.5的稀盐酸模拟胃酸过多时的胃液。将上述稀盐酸以相同的滴速分别滴入等质量两种药粉的悬浊液中,测得pH随滴入盐酸体积的变化如图所示。结合图像分析,铝碳酸镁片作为抗酸药除了能将胃液的pH保持在3~5之间,减少胃部不适,还具有的优势为___________(任填一条)。

三、实验与探究:本题共3小题,化学方程式及特殊标注每空2分,其余每空1分,共15分。
27. 云南斑铜“妙在有斑,贵在浑厚”,其制作技艺是国家非物质文化遗产。

(1)《滇南闻见录》记载:“自来铜(铜基合金),不可经火,须生锤成器”,通过捶打将斑铜塑成不同形状,体现了金属的___________性。斑铜的熔点比纯铜___________(填“高”或“低”)。
(2)斑铜主要含有铜、锌、锡、铁等。用如图所示装置及药品,通过一次实验验证锌、铁、铜的金属活动性,回答下列问题。

①组装好装置,装入药品前,应先___________。
②集气瓶中金属B和溶液X可能的组合为___________(任填一组)。
28. 为探究硫燃烧产物的性质,利用如图所示装置进行实验。
(1)实验室用过氧化氢溶液制取氧气,该反应的化学方程式为___________。
在集满氧气的三颈烧瓶中(夹持装置省略),加入少量紫色石蕊溶液,塞紧带电热棒和燃烧匙的双孔塞,关闭止水夹,引燃足量硫粉,充分反应。

资料卡片 I.通常状况下,1体积水约能溶解40体积SO2; II.SO2与CO2的化学性质相似。 |
(2)气球的作用是___________。
(3)燃烧结束,待装置冷却至室温,振荡烧瓶,紫色石蕊溶液变为___________色。打开止水夹,烧杯中可观察到的现象是___________。
29. 随着“碳中和”目标![]() 提出,CO2的捕集成为研究热点。氧化钙基吸附剂是目前CO2捕集技术中极具潜力的高温吸附剂。某研究团队对该固体吸附剂吸附性能的最佳改性条件展开探究。
提出,CO2的捕集成为研究热点。氧化钙基吸附剂是目前CO2捕集技术中极具潜力的高温吸附剂。某研究团队对该固体吸附剂吸附性能的最佳改性条件展开探究。
任务一:认识吸附剂的工作原理
【查阅资料1】
①吸附:CaO在高温下与CO2反应生成CaCO3;
②脱附:CaCO3焙烧分解生成CO2和CaO,实现CaO再生。
(1)CaO吸附CO2的化学方程式为___________。
在不同温度下,通过不同的溶剂与吸附剂产生相互作用,改变其比表面积等因素,可改良吸附剂的吸附性能。
任务二:探究溶剂种类和温度对吸附剂改性效果的影响
【实验探究】分别用75%的乙醇溶液和纯水在三个不同温度下,浸泡吸附剂进行改性。用等质量改性后的吸附剂进行吸附量的循环实验,得到吸附量与循环次数的关系如图所示。[已知:![]() ]
]
【查阅资料2】
①吸附剂每经过一次吸附和脱附为一个循环;
②吸附量越大,多次循环后吸附量越稳定,改性效果越好。

(2)由甲、乙两图可知:吸附剂的最佳改性条件为___________,理由是___________。
吸附剂吸附过程中,生成的CaCO3会覆盖在表面,阻止CO2的进一步扩散,造成吸附性能显著降低,蜂窝状多孔结构有利于CO2向吸附剂内部扩散和吸附。
任务三:探究吸附剂的孔结构对吸附效果的影响
【查阅资料3】
①Ca(OH)2与CO2反应制备CaCO3时,CO2流速会影响CaCO3的孔结构;
②由上述方法制得![]() CaCO3再制备CaO时,原有孔结构可以保留。
CaCO3再制备CaO时,原有孔结构可以保留。
(3)设计实验,探究用Ca(OH)2与CO2制备优质CaCO3原料的最佳条件___________。
【模型建构】探究多因素对某一变量的影响时,可采用控制变量法。
四、分析与计算:本题共1小题,共5分。
30. 高端芯片制造国产化是助力产业转型升级的重要支点。GaN是一种被广泛使用的半导体材料,合成纳米级GaN的原理之一为![]() 。若制得42g GaN,计算参加反应的Li3N的质量。
。若制得42g GaN,计算参加反应的Li3N的质量。
参考答案
一、选择题:本题共20小题,每小题2分,共40分。在每小题给出的四个选项中,只有一项是符合题目要求的。
【1题答案】
【答案】A
【2题答案】
【答案】B
【3题答案】
【答案】C
【4题答案】
【答案】A
【5题答案】
【答案】B
【6题答案】
【答案】A
【7题答案】
【答案】C
【8题答案】
【答案】A
【9题答案】
【答案】D
【10题答案】
【答案】D
【11题答案】
【答案】C
【12题答案】
【答案】C
【13题答案】
【答案】B
【14题答案】
【答案】B
【15题答案】
【答案】D
【16题答案】
【答案】C
【17题答案】
【答案】D
【18题答案】
【答案】C
【19题答案】
【答案】B
【20题答案】
【答案】C
二、填空与简答:本题共6小题,化学方程式每空2分,其余每空1分,共30分。
【21题答案】
【答案】(1)天然 (2)糖类 (3)C
(4)
保护并利用水资源,推进人与自然和谐共生。完成下面小题。
【22题答案】
【答案】(1)过滤 (2)明矾 (3)A (4)B
【23题答案】
【答案】(1)离子 (2) ①. 搅拌,加速溶解 ②. 不饱和
(3)减少 (4)耐腐蚀性
绘画是中华优秀传统文化的重要组成部分,许多绘画作品的背后都蕴含着现代化学的智慧。完成下面小题。
【24题答案】
【答案】(1)稳定 (2) ①. +3 ②. 3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
(3)H2O
【25题答案】
【答案】(1)搅拌,加快溶解速率
(2)确保把铁完全溶解
(3)
(4)将未反应对固体杂质除去,以免影响后续实验(合理即可)
【26题答案】
【答案】(1)3##三
(2) ①. 小苏打 ②. NaHCO3+2HCl=NaCl+H2O+CO2↑
(3)氢氧化铝片 (4)药效更稳定,持续时间更长;(合理即可)
三、实验与探究:本题共3小题,化学方程式及特殊标注每空2分,其余每空1分,共15分。
【27题答案】
【答案】(1) ①. 延展 ②. 低
(2) ①. 检查装置气密性 ②. Fe与稀硫酸(合理即可)
【28题答案】
【答案】(1)2H2O2![]() 2H2O+O2↑
2H2O+O2↑
(2)平衡瓶内压强 (3) ①. 红 ②. 烧杯中的NaOH倒吸入三颈烧瓶
【29题答案】
【答案】(1)
(2) ①. 75%乙醇(25℃) ②. 吸附量大,且多次循环后吸附量较稳定
(3)取多分等质量,等浓度的Ca(OH)2浆液,在相同温度和反应时间下,通入不同流速的CO2
四、分析与计算:本题共1小题,共5分。
【30题答案】
【答案】解:设参与反应的Li3N的质量为x

![]()
![]()
答:参与反应的Li3N的质量为17.5g。