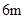2023年湖南普通高中学业水平选择性考试化学试题及答案
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 中华文化源远流长,化学与文化传承密不可分。下列说法错误的是
A. 青铜器“四羊方尊”的主要材质为合金
B. 长沙走马楼出土的竹木简牍主要成分是纤维素
C. 蔡伦采用碱液蒸煮制浆法造纸,该过程不涉及化学变化
D. 铜官窑彩瓷是以黏土为主要原料,经高温烧结而成
2. 下列化学用语表述错误的是
A. HClO的电子式:![]()
B. 中子数为10的氧原子:![]() O
O
C. NH3分子的VSEPR模型:
D. 基态N原子的价层电子排布图:
3. 下列玻璃仪器在相应实验中选用不合理的是

A. 重结晶法提纯苯甲酸:①②③ B. 蒸馏法分离CH2Cl2和CCl4:③⑤⑥
C. 浓硫酸催化乙醇制备乙烯:③⑤ D. 酸碱滴定法测定NaOH溶液浓度:④⑥
4. 下列有关物质结构和性质的说法错误的是
A. 含有手性碳原子的分子叫做手性分子
B. 邻羟基苯甲醛![]() 沸点低于对羟基苯甲醛的沸点
沸点低于对羟基苯甲醛的沸点
C. 酰胺在酸或碱存在并加热的条件下可发生水解反应
D. 冠醚(18-冠-6)的空穴与K+尺寸适配,两者能通过弱相互作用形成超分子
5. 下列有关电极方程式或离子方程式错误的是
A. 碱性锌锰电池的正极反应:MnO2+H2O+e-=MnO(OH)+OH-
B. 铅酸蓄电池充电时的阳极反应:Pb2++2H2O-2e-=PbO2+4H+
C. K3[Fe(CN)6]溶液滴入FeCl2溶液中:K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓
D. TiCl4加入水中:TiCl4+(x+2)H2O=TiO2・xH2O↓+4H++4Cl-
6. 日光灯中用到的某种荧光粉的主要成分为3W3(ZX4)2・WY2。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
A. 电负性:X>Y>Z>W
B. 原子半径:X<Y<Z<W
C. Y和W的单质都能与水反应生成气体
D. Z元素最高价氧化物对应的水化物具有强氧化性
7. 取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度均为![]() ),反应现象没有明显差别的是
),反应现象没有明显差别的是
选项 | 试剂① | 试剂② |
A | 氨水 |
|
B |
|
|
C |
| 酸性 |
D |
|
|
A. A B. B C. C D. D
8. 葡萄糖酸钙是一种重要的补钙剂,工业上以葡萄糖、碳酸钙为原料,在溴化钠溶液中采用间接电氧化反应制备葡萄糖酸钙,其阳极区反应过程如下:

下列说法错误的是
A. 溴化钠起催化和导电作用
B. 每生成![]() 葡萄糖酸钙,理论上电路中转移了
葡萄糖酸钙,理论上电路中转移了![]() 电子
电子
C. 葡萄糖酸能通过分子内反应生成含有六元环状结构的产物
D. 葡萄糖能发生氧化、还原、取代、加成和消去反应
9. 处理某铜冶金污水(含![]() )
)![]() 部分流程如下:
部分流程如下:

已知:①溶液中金属离子开始沉淀和完全沉淀的![]() 如下表所示:
如下表所示:
物质 |
|
|
|
|
开始沉淀 | 1.9 | 4.2 | 6.2 | 3.5 |
完全沉淀 | 3 | 6.7 | 8 | 4.6 |
②![]() 。
。
下列说法错误的是
A. “沉渣Ⅰ”中含有![]() 和
和![]()
B. ![]() 溶液呈碱性,其主要原因是
溶液呈碱性,其主要原因是![]()
C. “沉淀池Ⅱ”中,当![]() 和
和![]() 完全沉淀时,溶液中
完全沉淀时,溶液中
D. “出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水
10. 油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄![]() 褪色的主要原因是发生了以下两种化学反应:
褪色的主要原因是发生了以下两种化学反应:

下列说法正确的是
A. ![]() 和
和![]() 的空间结构都是正四面体形
的空间结构都是正四面体形
B. 反应Ⅰ和Ⅱ中,元素![]() 和S都被氧化
和S都被氧化
C. 反应Ⅰ和Ⅱ中,参加反应的 :Ⅰ<Ⅱ
:Ⅰ<Ⅱ
D. 反应Ⅰ和Ⅱ中,氧化![]() 转移的电子数之比为3∶7
转移的电子数之比为3∶7
11. 科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数为![]() 。阿伏加德罗常数的值为
。阿伏加德罗常数的值为![]() 。下列说法错误的是
。下列说法错误的是

A. 晶体最简化学式为![]()
B. 晶体中与![]() 最近且距离相等的
最近且距离相等的![]() 有8个
有8个
C. 晶胞中B和C原子构成的多面体有12个面
D. 晶体的密度为![]()
12. 常温下,用浓度为![]() 的
的![]() 标准溶液滴定浓度均为
标准溶液滴定浓度均为![]() 的
的![]() 和
和![]() 的混合溶液,滴定过程中溶液的
的混合溶液,滴定过程中溶液的![]() 随
随![]() (
( )的变化曲线如图所示。下列说法错误的是
)的变化曲线如图所示。下列说法错误的是

A. ![]() 约为
约为![]()
B. 点a:![]()
C. 点b:![]()
D. 水的电离程度:![]()
13. 向一恒容密闭容器中加入![]() 和一定量的
和一定量的![]() ,发生反应:
,发生反应:![]() 。
。![]() 的平衡转化率按不同投料比
的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列说法错误的是
随温度的变化曲线如图所示。下列说法错误的是

A. ![]()
B. 反应速率:![]()
C. 点a、b、c对应的平衡常数:![]()
D. 反应温度为![]() ,当容器内压强不变时,反应达到平衡状态
,当容器内压强不变时,反应达到平衡状态
14. ![]() 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某
是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某![]() (Ⅱ)催化剂(用
(Ⅱ)催化剂(用![]() 表示)能高效电催化氧化
表示)能高效电催化氧化![]() 合成
合成![]() ,其反应机理如图所示。
,其反应机理如图所示。

下列说法错误的是
A. ![]() (Ⅱ)被氧化至
(Ⅱ)被氧化至![]() (Ⅲ)后,配体
(Ⅲ)后,配体![]() 失去质子能力增强
失去质子能力增强
B. M中![]() 的化合价为
的化合价为![]()
C. 该过程有非极性键的形成
D. 该过程的总反应式:![]()
二、非选择题:本题共4小题,共58分。
15. 金属![]() 对
对![]() 有强吸附作用,被广泛用于硝基或羰基等不饱和基团的催化氢化反应,将块状
有强吸附作用,被广泛用于硝基或羰基等不饱和基团的催化氢化反应,将块状![]() 转化成多孔型雷尼
转化成多孔型雷尼![]() 后,其催化活性显著提高。
后,其催化活性显著提高。
已知:①雷尼![]() 暴露在空气中可以自燃,在制备和使用时,需用水或有机溶剂保持其表面“湿润”;
暴露在空气中可以自燃,在制备和使用时,需用水或有机溶剂保持其表面“湿润”;
②邻硝基苯胺在极性有机溶剂中更有利于反应的进行。
某实验小组制备雷尼![]() 并探究其催化氢化性能的实验如下:
并探究其催化氢化性能的实验如下:
步骤1:雷尼![]() 的制备
的制备

步骤2:邻硝基苯胺的催化氢化反应
反应的原理和实验装置图如下(夹持装置和搅拌装置略)。装置Ⅰ用于储存![]() 和监测反应过程。
和监测反应过程。

回答下列问题:
(1)操作(a)中,反应的离子方程式是_______;
(2)操作(d)中,判断雷尼![]() 被水洗净的方法是_______;
被水洗净的方法是_______;
(3)操作(e)中,下列溶剂中最有利于步骤2中氢化反应的是_______;
A. 丙酮 B. 四氯化碳 C. 乙醇 D. 正己烷
(4)向集气管中充入![]() 时,三通阀的孔路位置如下图所示:发生氢化反应时,集气管向装置Ⅱ供气,此时孔路位置需调节为_______;
时,三通阀的孔路位置如下图所示:发生氢化反应时,集气管向装置Ⅱ供气,此时孔路位置需调节为_______;

(5)仪器M的名称是_______;
(6)反应前应向装置Ⅱ中通入![]() 一段时间,目的是_______;
一段时间,目的是_______;
(7)如果将三颈瓶N中的导气管口插入液面以下,可能导致的后果是_______;
(8)判断氢化反应完全![]() 现象是_______。
现象是_______。
16. 聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
①![]()
②![]()
③![]()
计算反应④![]() 的
的![]() _______
_______![]() ;
;
(2)在某温度、![]() 下,向反应器中充入
下,向反应器中充入![]() 气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入_______
气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入_______![]() 水蒸气作为稀释气(计算时忽略副反应);
水蒸气作为稀释气(计算时忽略副反应);
(3)在![]() 、
、![]() 下,以水蒸气作稀释气。
下,以水蒸气作稀释气。![]() 作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
⑤![]()
⑥![]()
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S(![]() )随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是_______,理由是_______;
)随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是_______,理由是_______;

(4)关于本反应体系中催化剂![]() 的描述错误的是_______;
的描述错误的是_______;
A. X射线衍射技术可测定![]() 晶体结构
晶体结构
B. ![]() 可改变乙苯平衡转化率
可改变乙苯平衡转化率
C. ![]() 降低了乙苯脱氢反应的活化能
降低了乙苯脱氢反应的活化能
D. 改变![]() 颗粒大小不影响反应速率
颗粒大小不影响反应速率
Ⅱ.苯乙烯的聚合
苯乙烯聚合有多种方法,其中一种方法的关键步骤是某![]() (Ⅰ)的配合物促进
(Ⅰ)的配合物促进![]() (引发剂,X表示卤素)生成自由基
(引发剂,X表示卤素)生成自由基![]() ,实现苯乙烯可控聚合。
,实现苯乙烯可控聚合。
(5)引发剂![]() 中活性最高的是_______;
中活性最高的是_______;
(6)室温下,①![]() 在配体L的水溶液中形成
在配体L的水溶液中形成![]() ,其反应平衡常数为K;②
,其反应平衡常数为K;②![]() 在水中的溶度积常数为
在水中的溶度积常数为![]() 。由此可知,
。由此可知,![]() 在配体L的水溶液中溶解反应的平衡常数为_______(所有方程式中计量系数关系均为最简整数比)。
在配体L的水溶液中溶解反应的平衡常数为_______(所有方程式中计量系数关系均为最简整数比)。
17. 超纯![]() 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯
是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯![]() 方面取得了显著成果,工业上以粗镓为原料,制备超纯
方面取得了显著成果,工业上以粗镓为原料,制备超纯![]() 的工艺流程如下:
的工艺流程如下:

已知:①金属![]() 的化学性质和
的化学性质和![]() 相似,
相似,![]() 的熔点为
的熔点为![]() ;
;
②![]() (乙醚)和
(乙醚)和![]() (三正辛胺)在上述流程中可作为配体;
(三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:
物质 |
|
|
|
|
沸点/ | 55.7 | 34.6 | 42.4 | 365.8 |
回答下列问题:
(1)晶体![]() 的晶体类型是_______;
的晶体类型是_______;
(2)“电解精炼”装置如图所示,电解池温度控制在![]() 的原因是_______,阴极的电极反应式为_______;
的原因是_______,阴极的电极反应式为_______;

(3)“合成![]() ”工序中的产物还包括
”工序中的产物还包括![]() 和
和![]() ,写出该反应的化学方程式:_______;
,写出该反应的化学方程式:_______;
(4)“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是_______;
(5)下列说法错误的是_______;
A. 流程中![]() 得到了循环利用
得到了循环利用
B. 流程中,“合成![]() ”至“工序X”需在无水无氧的条件下进行
”至“工序X”需在无水无氧的条件下进行
C. “工序X”的作用是解配![]() ,并蒸出
,并蒸出![]()
D. 用核磁共振氢谱不能区分![]() 和
和![]()
(6)直接分解![]() 不能制备超纯
不能制备超纯![]() ,而本流程采用“配体交换”工艺制备超纯
,而本流程采用“配体交换”工艺制备超纯![]() 的理由是_______;
的理由是_______;
(7)比较分子中的![]() 键角大小:
键角大小:![]() _______
_______![]() (填“>”“<”或“=”),其原因是_______。
(填“>”“<”或“=”),其原因是_______。
18. 含有吡喃萘醌骨架的化合物常具有抗菌、抗病毒等生物活性,一种合成该类化合物的路线如下(部分反应条件已简化):

回答下列问题:
(1)B的结构简式为_______;
(2)从F转化为G的过程中所涉及的反应类型是_______、_______;
(3)物质G所含官能团的名称为_______、_______;
(4)依据上述流程提供的信息,下列反应产物J的结构简式为_______;

(5)下列物质的酸性由大到小的顺序是_______(写标号):
①![]() ②
②![]() ③
③![]()
(6)![]() (呋喃)是一种重要的化工原料,其能够发生银镜反应的同分异构体中。除H2C=C=CH-CHO外,还有_______种;
(呋喃)是一种重要的化工原料,其能够发生银镜反应的同分异构体中。除H2C=C=CH-CHO外,还有_______种;
(7)甲苯与溴在FeBr3催化下发生反应,会同时生成对溴甲苯和邻溴甲苯,依据由C到D的反应信息,设计以甲苯为原料选择性合成邻溴甲苯的路线_______(无机试剂任选)。
参考答案
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
【1题答案】
【答案】C
【2题答案】
【答案】C
【3题答案】
【答案】A
【4题答案】
【答案】D
【5题答案】
【答案】B
【6题答案】
【答案】C
【7题答案】
【答案】D
【8题答案】
【答案】B
【9题答案】
【答案】D
【10题答案】
【答案】D
【11题答案】
【答案】C
【12题答案】
【答案】D
【13题答案】
【答案】B
【14题答案】
【答案】B
二、非选择题:本题共4小题,共58分。
【15题答案】
【答案】(1)2Al+2OH-+2H2O=2AlO![]() +3H2↑
+3H2↑
(2)取最后一次洗涤液于试管中,滴加几滴酚酞,如果溶液不变粉红色,则证明洗涤干净,否则没有洗涤干净 (3)C
(4)C (5)恒压滴液漏斗
(6)排除装置中的空气,防止雷尼![]() 自燃
自燃
(7)管道中气流不稳,不利于监测反应过程
(8)集气管中液面不再改变
【16题答案】
【答案】(1)+118
(2)5 (3) ①. 苯 ②. 反应④为主反应,反应⑤⑥为副反应,苯乙烯的选择性最大;在恒温恒压下,随乙苯转化率的增大,反应⑤正向移动,反应⑥不移动,则曲线b代表产物苯 (4)BD
(5)C6H5CH2Cl
(6)K?Ksp
【17题答案】
【答案】(1)分子晶体
(2) ①. 保证Ga为液体,便于纯Ga流出 ②. Ga3++3eˉ=Ga
(3)8CH3I+2Et2O+Ga2Mg5=2![]() +3
+3![]() +2
+2![]() ;
;
(4)CH4 (5)D
(6)NR3沸点较高,易与Ga(CH3)3分离,Et2O的沸点低于Ga(CH3)3,一起气化,难以得到超纯Ga(CH3)3
(7) ①. > ②. Ga(CH3)3中Ga为sp2杂化,所以为平面结构,而Ga(CH3)3(Et2O)中Ga为sp3杂化,所以为四面体结构,故夹角较小
【18题答案】
【答案】(1) (2) ①. 消去反应 ②. 加成反应
(2) ①. 消去反应 ②. 加成反应
(3) ①. 碳碳双键 ②. 醚键
(4) (5)②>③>①
(5)②>③>①
(6)4 (7)![]()
![]()

![]()

![]()

-

2024年湖南普通高中学业水平合格性考试成绩查询入口:https://w
2024-07-04 -

2024年湖南普通高中学业水平选择性考试化学试题及答案
2024-06-26 -
2024年湖南普通高中学业水平选择性考试物理试题及答案
2024-06-22 -

2024年湖南普通高中学业水平选择性考试地理试题及答案
2024-06-22 -

2023年湖南学考合格考成绩查询入口(已开通)
2023-07-31 -

2023年湖南普通高中学业水平合格性考试成绩查询入口(已开通)
2023-07-27 -

2023年湖南普通高中学业水平选择性考试政治试题及答案
2023-07-12 -

2023年湖南普通高中学业水平考试准考证打印入口网站:https://w
2023-06-29